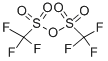
| Kirjeldus |
Trifluorometaansulfoonanhüdriid, tuntud ka kui trifluorometaansulfoonanhüdriid, on osutunud erakordseks reagendiks paljude transformatsioonide jaoks. Kaubanduslikult ja kergesti saadaoleva reagendina on seda kõrge elektrofiilsuse tõttu laialdaselt kasutatud sünteetilises keemias. Arvestades selle kõrget afiinsust O-nukleofiilide suhtes, on reaktsioonid alkoholide, karbonüülide, väävelfosfor- ja joodoksiididega tugevalt eelistatud vastavate triflaatide moodustumiseks. Olles üks peamisi lahkuvaid rühmi orgaanilises keemias, avavad tekkinud triflaadid ukse erinevatele allavoolu muundumistele, sealhulgas (kuid mitte ainult) asendusreaktsioonidele, ristsidestusprotsessidele, redoksreaktsioonidele ja ümberkorraldustele[1-2] . |
| Keemilised omadused |
selge värvitu kuni helepruun vedelik |
| Kasutab |
Trifluorometaansulfoonanhüdriid on tugev elektrofiil, mida kasutatakse keemilises sünteesis triflüülrühma sisestamiseks. |
| Kasutab |
Trifluorometaansulfoonanhüdriidi kasutatakse fenoolide ja imiini muundamiseks trifluorestriks ja NTf rühmaks. See on tugev elektrofiil, mida kasutatakse triflüülrühma sisestamiseks keemilises sünteesis. See toimib reagendina alküül- ja vinüültriflaatide valmistamisel ning mannosasiidmetüüluronaadi doonorite stereoselektiivsel sünteesil. See toimib polüsahhariidide valmistamiseks anomeersete hüdroksüsuhkrutega glükosüülimise katalüsaatorina. |
| Definitsioon |
ChEBI: Triflic anhüdriid on organosulfoonanhüdriid. See on funktsionaalselt seotud trifliinhappega. |
| Reaktiivsuse profiil |
Tertsiaarsete ja sekundaarsete amiidide elektrofiilne aktiveerimine trifluorometaananhüdriidiga (Tf2O; rifluorometaansulfoonanhüdriid) pehmetes tingimustes tekitab vastavalt imiiniumi ja iminotriflaate, mida saab kasutada mitmekülgsete reagentidena reageerimiseks erinevate C-, N-, O- ja S-ga. -nukleofiilid amiidfunktsiooni muundamiseks erinevateks produktideks. Teised hapnikku sisaldavad nukleofiilid, nagu sulfoksiidid ja fosforoksiidid, võivad samuti läbida Tf2O-ga nukleofiilse rünnaku, et tekitada tioontriflaati, elektrofiilseid P-liike ja fosfooniumtriflaati. Need väga aktiivsed mööduvad liigid võivad kergesti läbida nukleofiilseid asendusreaktsioone edasiste erinevate transformatsioonide jaoks. Lisaks on Tf2O tugeva elektrofiilse omaduse tõttu altid reageerima suhteliselt nõrkade nukleofiilidega, nagu nitriilrühmad või mõned lämmastikku sisaldavad heterotsüklilised ühendid. Lisaks on Tf2O-d kasutatud ka tõhusa radikaalse trifluorometüülimise ja trifluorometüültioolimise reagendina SO2 vabastamise või desoksügeenimisprotsessi kaudu trifluorometüülitud ja trifluorometüültioolitud ühendite sünteesiks[2]. |
| Oht |
Võib olla metalle söövitav. Kahjulik allaneelamisel. Põhjustab raskeid nahapõletusi ja silmakahjustusi. |
| Süttivus ja plahvatusohtlikkus |
Pole klassifitseeritud |
| Süntees |
Trifluorometaansulfoonanhüdriidi süntees on järgmine:
Kuiva, {{0}} ml, ümarapõhjalisse kolbi täidetakse 36,3 g. (0,242 mol) trifluorometaansulfoonhapet (märkus 1) ja 27,3 g. (0,192 mol) fosforpentoksiidi (märkus 2). Kolb suletakse korgiga ja lastakse toatemperatuuril seista vähemalt 3 tundi. Selle aja jooksul muutub reaktsioonisegu suspensioonist tahkeks massiks. Kolb on varustatud lühikese teega destilleerimispeaga ja seda kuumutatakse esmalt kuuma õhuvooluga kuumapüstolist ja seejärel väikese põleti leegiga.Kolbi kuumutatakse, kuni trifluorometaansulfoonanhüdriid enam ei destilleerub, keetja 82–115 kraadi, saades 28,4–31,2 g. (83–91%) anhüdriidist, värvitu vedelik. Kuigi see toode on järgmises etapis kasutamiseks piisavalt puhas, võib järelejäänud happe anhüdriidist eemaldada järgmise protseduuriga. 3,2 g läga. fosforpentoksiidi 31,2 g. tooranhüdriidi segatakse toatemperatuuril korgiga kolvis 18 tundi. Pärast seda, kui reaktsioonikolb on varustatud lühitee destilleerimispeaga, kuumutatakse seda õlivannis, saades 0,7 g. esiosa, bp 74–81 kraadi, millele järgneb 27,9 g. puhtast trifluorometaansulfoonhappe anhüdriidist, bp 81–84 kraadi.

|
| ladustamine |
Hoida jahedas, kuivas, hästiventileeritavas kohas. Niiskustundlik. |
| Puhastusmeetodid |
Seda saab värskelt valmistada veevabast happest (11,5 g) ja P2O5-st (11,5 g ehk pool sellest massist), jättes 1 tunniks toatemperatuuril kõrvale, destilleerides välja lenduvad saadused ja destilleerides seejärel läbi lühikese Vigreux kolonni. Seda hüdrolüüsib kergesti H2O ja see laguneb märgatavalt mõne päeva pärast, vabastades SO2 ja moodustades viskoosse vedeliku. Hoida kuivas madalal temperatuuril. [Burdon et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Viited |
[1] Haoqi Zhang. "Trifluorometaansulfoonanhüdriid amiidi aktiveerimisel: võimas tööriist heterotsükliliste südamike sepistamiseks." TCIMAIL (2021).
[2] Dr Qixue Qin, prof dr Ning Jiao, Zengrui Cheng. "Trifluorometaansulfoonanhüdriidi hiljutised rakendused orgaanilises sünteesis." Angewandte Chemie 135 10 (2022). |